2017 國際同行評審會議報告:科研刊物的報告質量

【意得輯企業溝通經理 Hridey Manghwani 正在美國芝加哥出席 2017 國際同行評審會議,以下是由 Hridey 觀點寫成的第二天會議報告。】
在 Ottawa Hospital Research Institute 的 David Moher 的主題演講結束后,第八屆國際同行評審和科研發表會議第二天的議程便正式展開,今天的重點是報告質量。渥太華大學?Robert Frank 報告了他所屬團隊的研究,分析影像研究中錯誤結果相關的變量。薈萃分析 (meta analyses, MAs) 是影像研究中最接近真實的代表,團隊研究了研究層級(相對 STARD 的引用率、發表順序和發表時間)和期刊層級的變量(影響因子、STARD 認可和引用半衰期)與?MAs 中主要研究結果和概要估計間的距離的關系。在分析了 98 篇包含 1458 個主要研究的 MAs 后,得出以下結論,發表在影響因子 (IF) 較低的期刊的 MAs 中主要研究結果和概要估計間的距離并不小于發表在高影響因子期刊上的研究。他們的結論再次強調高影響因子和高引用率并不代表研究質量比較好。

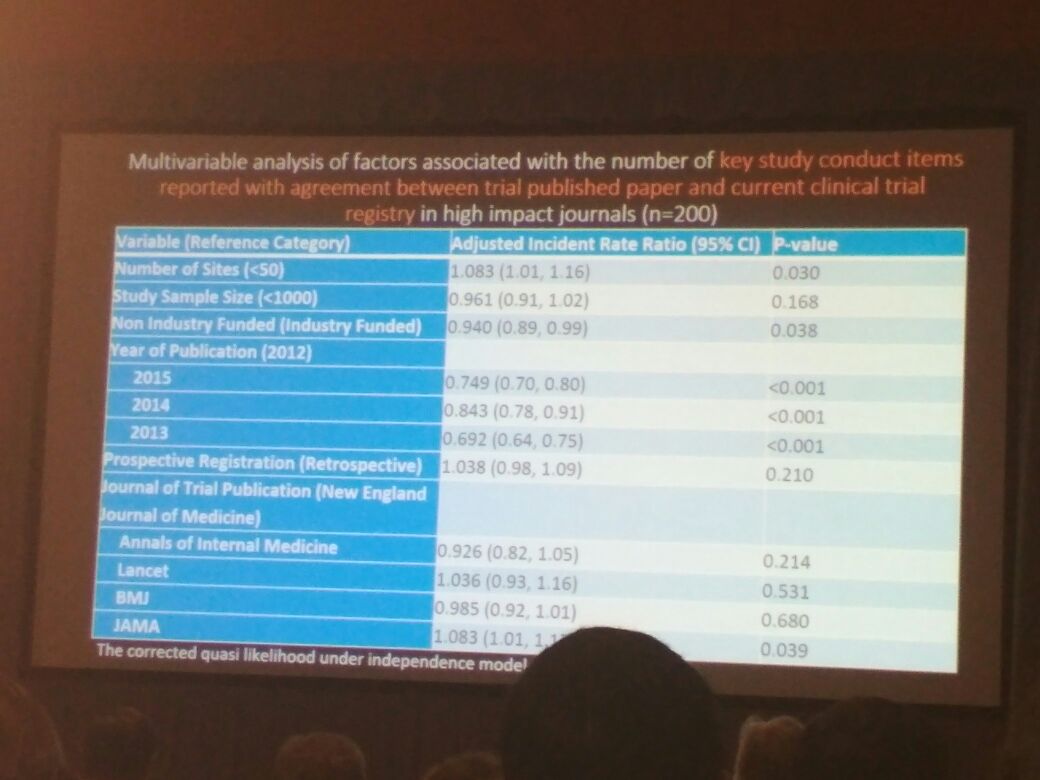
接下來是加拿大麥克馬斯特大學、Toronto General Hospital Health Network 的 Sarah Daisy Kosa 帶來的研究:發表的試驗數據與發表在高影響因子期刊上的已注冊臨床試驗間的差距,她的團隊在?PubMed?上檢索 2012 至 2015 年間,所有發表在影響因子排名前五的醫學期刊(根據 2014 湯森路透期刊引證報告)上的隨機臨床試驗 (randomized clinical trials, RCTs),在團隊研究 200 份 RCT 中,發現發表文章和臨床試驗注冊存在差距,研究清楚指出,要保持科學研究質量與誠信,需要統一發表的臨床數據報告和注冊。
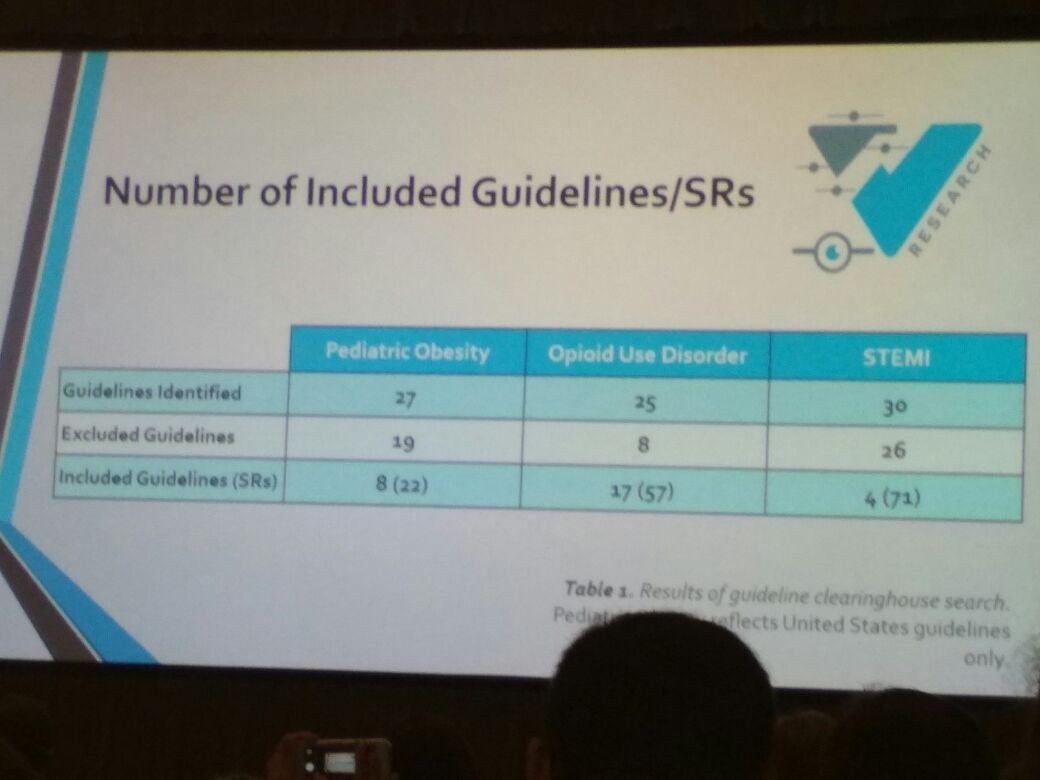
接著,美國俄克拉荷馬州立大學健康科學中心的 Cole Wayant 在臨床實踐指南的準則上,討論了系統綜述 (systematic reviews, SRs) 方法和報告的質量。他的研究用?PRISMA?(Preferred Reporting Items for Systematic Reviews and Meta-analyses) 和?AMSTAR?(A Measurement tool to assess Systematic Reviews)?分析了 MAs 和 SRs,研究結果顯示 MAs 和 SRs 皆缺少這些檢查清單中的許多項目,凸顯需要提升 SRs 質量的必要性,特別是 SRs 屬于 1A 等級證據,可以影響臨床決策,進而影響循證醫學。
最后或許也是互動性最強的課堂是由美國加利福尼亞大學住院醫師 Kaveh Zakeri 帶來的簡報,他的研究分析了當前 National Clinical Trials Network 3 期試驗存有的樂觀偏見。Zakeri 的團隊從 PubMed 找出 2007 年 1 月至 2017 年 1 月間 185 篇 3 期隨機對照臨床試驗,比較提出的效應量和觀察到的效應量,他們計算了兩者風險比 (hazard ratios, HRs),風險比具有比較高的治療效果和減少不良反應指標性,結果顯示大部分 NCI 資助的 3 期試驗的新療法并沒有達到統計顯著性。他們建議,雖然樂觀偏見的幅度已經比 1955 至 2006 年的試驗減少,但臨床試驗 protocol 還是需要更合理地提出效應量。許多窄門領域中的試驗無法重復,甚至因為無法招募到足夠的病患導致樣本量極小,大部分 2 期和 3 期的試驗對提出的效應量都沒有合理的說明。
我們將在下一篇會議報告中報告下午的議程,下午的議程討論了科研文獻、試驗注冊和基金審查。
?
意得輯專家視點 2017?國際同行評審會議報告:






